近日,我校william威廉中文朱蓓薇院士团队陈翊平教授课题组在食源性致病菌快速检测方面的最新研究成果以“Activation Mechanism and Integrated One-Pot Assay of Chiral-like crRNA-Enhanced CRISPR/Cas12a Systems”为题在《Nature Communications》上发表。该研究明确了CRISPR/Cas12a体系中pre-crRNA成熟过程中释放的5′端重复片段的独特功能,构建了首个基于“延迟剪切”特性的一锅法检测方法,实现了海产品中多种食源性致病菌准确快速检测,为保障海洋食品安全提供有力工具。此项成果刊发于《Nature》子刊,彰显了我校在食品科学基础研究领域的显著实力与重要突破,也充分体现了学校科研创新能力持续跃升。
近年来,学校始终坚守立德树人根本任务,主动对接国家重大战略需求,扎实推进科研工作高质量内涵式发展。本次成果的取得,正是学校深耕基础研究、强化原始创新的重要体现,为相关学科建设与科研水平提升注入强劲动力。

研究简介:海产品中食源性致病菌的快速精准检测对保障食品安全至关重要。CRISPR/Cas12a系统作为兼具RNase与DNase活性的V型效应蛋白,已在食源性致病菌快速检测领域中发挥了核心作用。然而,pre-crRNA成熟过程中释放的5′端重复片段是否具有独特功能尚不明确,是亟待解决的关键科学问题。此外,扩增体系与Cas12a检测体系间的天然不兼容性,阻碍了单管高效反应及现场快速检测应用。因此,开发新型一锅法检测策略,实现扩增与切割反应的兼容,避免气溶胶污染,对提升Cas12a核酸分析方法在食源性致病菌检测中的准确性与实用性具有重要意义。
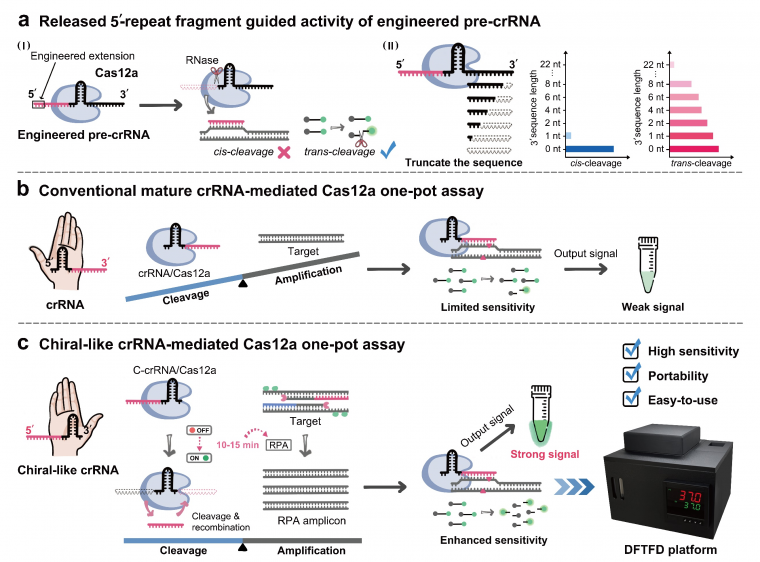
研究原理图
研究发现,工程化的5'端重复片段能够有效激活Cas12a的切割活性,其切割效率强烈依赖于3'端间隔区的序列长度。值得注意的是,当3'端间隔区完全截短时,会形成一种“类手性crRNA”构象,从而引导出一种延迟切换模式的Cas12a激活机制,这与传统的成熟crRNA截然不同。基于这一特性,该团队开发了一种基于延迟切割特征的一锅法传感策略,以应对长期以来基于Cas12a的切割反应与核酸扩增不相容的难题,其灵敏度相较于传统的成熟crRNA介导的一锅法提升了1,000倍。此外,将基于切割的一锅法检测与便携式温控荧光成像设备整合,构建了一个用于高通量筛查的现场诊断平台,实现了海产品中多种致病菌的准确快速检测。该研究进一步深化了对crRNA引导机制的理解,并推动了其在基因编辑和分子诊断领域应用范围的拓展。
该研究工作依托于william威廉中文和海洋食品加工与安全控制全国重点实验室两个平台完成,得到了国家自然科学基金项目的支持。论文第一作者为williamhill威廉希尔2024级博士研究生李永辉,通讯作者为williamhill威廉希尔陈翊平教授。
论文链接:https://www.nature.com/articles/s41467-026-71675-7
文字/陈翊平
图片/陈翊平
编辑/杜静
审核/杜静、牟俊、秦磊


